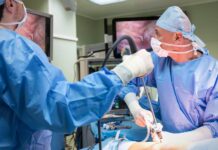
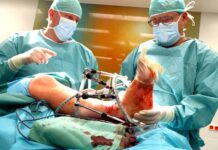
Pokračovat v účasti na klinickém testování léčiv není pro uprchlíky v ČR problém. S přesunem do hodnocení zapojeného účastníka z Ukrajiny ale musí souhlasit zadavatel hodnocení. Na podmínky upozorňuje Státní ústav pro kontrolu léčiv.
Převést účastníka klinického hodnocení léčivého přípravku z centra na Ukrajině do centra v Česku není podle Státního ústavu pro kontrolu léčiv [SÚKL] nijak složité. Konečné rozhodnutí vždy ale vyslovuje zadavatel daného klinického hodnocení.
„Zákon o léčivech a nařízení 536/2014, ICH E6 (R2) Good Clinical Practice nevylučují zařazování cizinců do klinických hodnocení, ani přesun subjektu hodnocení z centra klinického hodnocení do jiného centra,“ potvrzuje v doplňujících informacích k podmínkám klinického hodnocení léčiv Státní ústav pro kontrolu léčiv [SÚKL].
O pomoc při hledání centra v Česku, kde klinické hodnocení probíhá, se zájemci obracejí na následující kontakt: office@aifp.cz.
Druhou možností je pak oslovit Odbor klinického hodnocení léčivých přípravků SÚKL na následujících emailových adresách:
- natalie.bockova@sukl.cz
- alice.nemcova@sukl.cz
Od čtvrtka 17. března se pro zájemce o zapojení nebo pokračování v klinických hodnocení aktivuje navíc telefonní číslo 272 185 884.
Účast na testování léčiv musí cizinec nějak prokázat
Lékový regulátor dále upozorňuje, že přesun subjektu hodnocení [účastníka] nebo zařazení cizince do nového klinického hodnocení v Česku musí být vždy v jeho zájmu. Podmínkou pak je, že s takovým postupem souhlasí i zadavatel hodnocení.
„Proto lze v opodstatněných případech, jakými je situace na Ukrajině, této možnosti využít,“ potvrzuje na svých webových stránkách SÚKL.
Pokračování v účasti na klinickém hodnocení, které daný uprchlík započal ještě na Ukrajině, podmiňuje prokázání alespoň některých údajů o testování. Podle SÚKL je třeba předložit číslo protokolu o klinickém hodnocení. Dále název hodnoceného přípravku, diagnózu, pro kterou žadatele do klinického hodnocení instituce zařadila. Anebo stačí doložit alespoň název zadavatele, tedy společnosti, která hodnocení provádí.
Ideální je kartička účastníka klinického hodnocení. Případně léky, u nichž bude možné získat více informací z označení na obalu. Byť to není podmínka, informuje lékový regulátor. Nicméně čím více informací instituce získají, tím snáze a rychleji dokáží vyhledat dané klinické hodnocení.
Klinická hodnocení dokazují bezpečnost a účinnost léčiva
Dříve než výrobce uvede nějaký lék na trh, čeká ho obvykle i několikaletý výzkum. Výsledky z něj pak mají prokázat, že jde skutečně o kvalitní, účinný a bezpečný lék.
Navíc klinická hodnocení prováděná na lidech podléhají velmi přísným pravidlům a vždy mají předem určený plán testování. Ještě před samotnými klinickými testy se přípravek ověřuje na zvířatech nebo buněčných kulturách. Což se nazývá preklinické testování. Při něm vědci testují například akutní a chronickou toxicitu, karcinogenitu, mutagenitu a další nežádoucí účinky.
Každou žádost o provedení klinického hodnocení u nás nejdříve posuzuje a odsouhlasuje SÚKL a zároveň i minimálně jedna etická komise.
„Posuzuje se splnění požadavků na správnou klinickou praxi. Což je standard pro plánování, provádění, vedení, monitorování a další činnosti, které zajistí věrohodné a přesné údaje, ochranu práv a integritu osob zařazených do klinického hodnocení i důvěrnost jejich údajů,“ popisuje lékový ústav.
Součástí schvalovacího řízení je také zhodnocení poměru možných rizik a přínosů léku pro pacienty. Dále i vědecké opodstatnění klinického hodnocení a kvalita používaných léků.
–VRN–