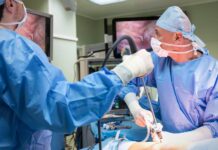
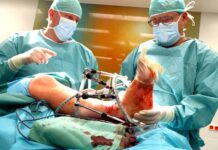
Vakcína od Pfizer a BioNTech je první plnohodnotně schválená očkovací látka proti covidu-19 ve Spojených státech. O její plné registraci včera [23.8.] rozhodl americký Úřad pro kontrolu potravin a léčiv [FDA].
Informaci o schválení vakcíny přinesl americký list The Washington Post. Očkovací látka byla do té doby stejně jako v Evropské unii [EU] schválena pouze k nouzovému použití. Podle některých odborníků pomůže tento krok upevnit důvěru americké veřejnosti k očkování proti covidu-19. Spojené státy totiž aktuálně opět čelí nárůstu počtu infekcí. V populaci nyní převažuje rychlejší delta mutace viru a její varianty.
„Zatímco miliony lidí už bezpečně dostaly vakcínu proti covidu-19, chápeme, že schválení vakcíny FDA může lidem dodat vůči očkování důvěru,“ uvedla komisařka FDA Janet Woodcocková.
Comirnaty v USA dostalo přes 204 milionu lidí
Očkovací látka známá jako Comirnaty byla ve Spojených státech schválena k nouzovému použití loni v prosinci. Podle údajů ze soboty 21. srpna ji od té doby dostalo přes 204 milionů lidí. Proočkovanost Američanů nyní dosahuje zhruba 51 procent.
„Veřejnost si může být jista, že tato vakcína splňuje vysoké standardy bezpečnosti, účinnosti a kvality výroby, které FDA po schváleném produktu požaduje,“ ubezpečila veřejnost komisařka.
Udělení licence od FDA ocenil včera na Twitteru i jeden ze dvou výrobců této vakcíny a sice firma BioNTech.
„FDA schválila naši žádost o udělení licence mRNA vakcíně k prevenci onemocnění covid-19 u osob straších 16 let. Rozhodnutí ji činí první vakcínou proti covidu-19 v USA plně schválenou tímto úřadem,“ reagoval po zveřejnění rozhodnutí německý výrobce BioNTech, který při vývoji a produkci vakcíny již na počátku pandemie spojil své síly s americkou farmaceutickou firmou Pfizer.
Pfizer/BioNTech v USA očkuje od prosince 2020
Americký regulátor původní nouzové schválení udělil výrobcům na základě klinické studie, která po dobu nejméně dvou měsíců zkoumala 44 tisíc lidí starších 16 let. Pfizer následně ve studii pokračoval. Americký úřad se kromě toho při posudku opíral také o důkazy z použití vakcíny mimo klinické testování.
Za upozornění stojí, že vakcína je nyní plně schválena pro osoby starší 16 let. Pro mladistvé od 12 do 15 let je očkovací látka registrovaná stále jen pro nouzové použití.
Podle FDA jsou závažné vedlejší účinky vakcíny, jako například bolesti na hrudníku či zánět srdečního svalu u dospívajících a mladších dospělých, stále mimořádně vzácné. Výsledky šest měsíců trvající studie dokládají, že vakcína Pfizer/BioNTech má vůči závažnému průběhu nemoci covid-19 účinnost až 97 procent. Ochrana proti mírnému průběhu je nejvyšší zhruba dva měsíce po druhé dávce [96 procent]. Po šesti měsících dosahuje ochrany kolem 84 procent.
Agentura AP ale také připomíná, že zmíněné údaje vychází z doby před tím, než se začala po světě šířit nakažlivější varianta delta. Jiná data z amerického Střediska pro kontrolu a prevenci nemocí [CDC] avšak ukazují, že vakcína je účinná i proti této variantě.
–ČTK/VRN–