Kontrola kvality očkovací látky vezme více než dvě třetiny doby z celého výrobního procesu. Na bezpečnost a účinnost všech v unijních zemích registrovaných vakcín dohlíží výrobce, kontrolní laboratoře i lékové úřady.
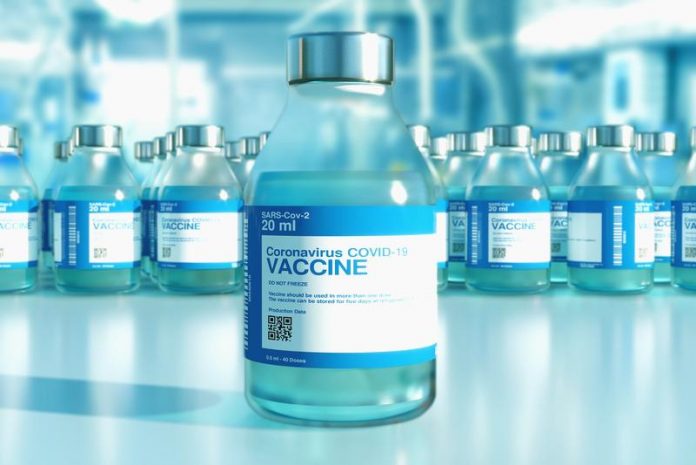
Výroba očkovací látky trvá v průměru dvanáct až 36 měsíců v závislosti na technologii její výroby. Typ vakcíny pak určí podmínky jejího skladování a další redistribuce [mRNA, vektorová či proteinová vakcína]. Samotný výrobní proces je pak vždy detailně popsaný v registrační dokumentaci očkovací látky. Kontrola její kvality a tedy i bezpečnosti zabere výrobci, Evropské agentuře pro léčivé přípravky [EMA] a dalším laboratořím až 70 procent celé doby výroby.
„Kontroluje se vždy šarže. Její velikost a objem se liší dle konkrétní vakcíny. Kontrola probíhá na straně výrobce, v souladu s registrační dokumentací pro Evropskou lékovou agenturu, i v nezávislé certifikované úřední kontrolní laboratoři léčiv,“ popisuje výkonný ředitel Asociace inovativního farmaceutického průmyslu [AIFP] Jakub Dvořáček.
Šarže je vlastně množství látky vyrobené nebo připravené v jednom výrobním cyklu, anebo postupu. Obvykle jde o tisíce dávek očkovací látky. Přesněji šarži definuje Zákon o léčivech.
Kontrola vakcín v kritických bodech výroby
Již při vývoji vakcíny výrobce pravidelně kontroluje již předem určené kritické kroky. Pro každý takový krok se již stanoví rozptyl výsledných hodnot. Pokud se při sledování těchto dat zjistí jejich překročení, celá šarže se zlikviduje. Výrobce látky pak upraví její produkci.
„Popis celého procesu, včetně kritických kroků, je součástí registrační dokumentace, která byla poskytnuta EMA jako podklad pro registraci,“ doplňuje AIFP ve své zprávě.
Upozorňuje dále, že výrobce vakcín musí být držitelem povolení k výrobě, striktně dodržovat požadavky legislativy a správné výrobní praxe. Navíc ho mohou kdykoli zkontrolovat inspektoři národní lékové autority.
Kontroluje se i každá šarže mířící mezi lidi
Bezpečnost vakcín zajišťují lékové instituce další kontrolou jednotlivé šarže ještě před tím, než ji výrobce uvede na samotný trh. Ověřuje především to, jestli látky z dané šarže souhlasí s registračními dokumenty a zároveň se zapisují do centrálního registru EU. Ještě před distribucí vakcín na trh kontroluje danou šarži i nezávislá certifikovaná laboratoř léčiv. Ta je vždy součástí sítě evropských úředních kontrolních laboratoří léčiv [OMCL].
„Laboratorní odbor SÚKL je členem sítě evropských úředních kontrolních laboratoří. Úřední propouštění šarží vakcín a krevních derivátů probíhá na základě laboratorního přezkoušení vybraných parametrů daného léčivého produktu a kontrole dokumentace šarže vydáním evropského certifikátu a propouštěním do oběhu v EU,“ vysvětluje ředitelka Státního ústavu pro kontrolu léčiv [SÚKL] Irena Storová.
Teprve po přezkoušení konkrétní šarže očkovací látky laboratoří z OMCL se vakcína pustí do oběhu členského státu. A dostává se k samotným pacientům.
Skladování a přeprava vakcín se stále sledují
Součástí zajištění účinnosti a bezpečnosti léčivých přípravků je jejich správné skladování a distribuce. Přičemž každá očkovací látka vyžaduje o něco jiné podmínky při manipulaci s ní i jejím uchovávání. To vše je podrobně popsané v její registrační dokumentaci.
„Genetické RNA vakcíny musí být transportovány i skladovány pod bodem mrazu, nebo dokonce při hlubokém zmražení z důvodů mechanické křehkosti RNA i jejímu snadnému rozkladu všudypřítomnými enzymy ribonukleázami,“ upřesňuje ředitel Biologického centra Akademie věd ČR Libor Grubhoffer.
Oproti tomu vektorové vakcíny na bázi rekombinantních adenovirových částic jsou podle něj díky přirozené stabilitě DNA mnohem odolnější vůči mechanickým i teplotním vlivům. Jejich transport a skladování jsou možné při chladničkové teplotě nad bodem mrazu.
Převoz vakcín do místa očkování není jednoduchý
Dodávky přepravující vakcíny mají měřidlo, které sleduje teplotní režim po celou dobu přepravy. Pokud dojde k teplotnímu výkyvu, automaticky se spustí alarm. Výrobce po takovém upozornění posuzuje, jestli nedošlo k ohrožení kvality, bezpečnosti a účinnosti přepravované várky vakcín.
„Teplotní řetězec monitorujeme nepřetržitě od převzetí na naše distribuční centrum, až po předání ‚do rukou‘ poskytovatele zdravotních služeb,“ tvrdí předseda představenstva společnosti Avenier Tomáš Florian, která u nás očkovací látky proti covidu-19 rozváží.
S tím souvisí i riziko nákupu očkovacích látek proti covidu-19 nabízených na internetu. Na což již několikrát upozornil také Interpol. Právě u takových látek jsou rizika spojená s nedodržením správného výrobního procesu, skladování či distribucí obrovská.
„Může se jednat o vakcíny se zcela jiným složením nebo přípravky z neschválených zdrojů bez certifikace správné výrobní praxe, hrozí u nich také neověřitelnost podmínek při skladování a distribuci,“ varuje závěrem Jakub Dvořáček.
–VRN–